Il nuovo discusso farmaco contro l’Alzheimer
L'Aduhelm è stato approvato da poco negli Stati Uniti: secondo l'azienda che lo produce potrebbe migliorare la vita a milioni di malati, ma ci sono forti dubbi sulla sua efficacia
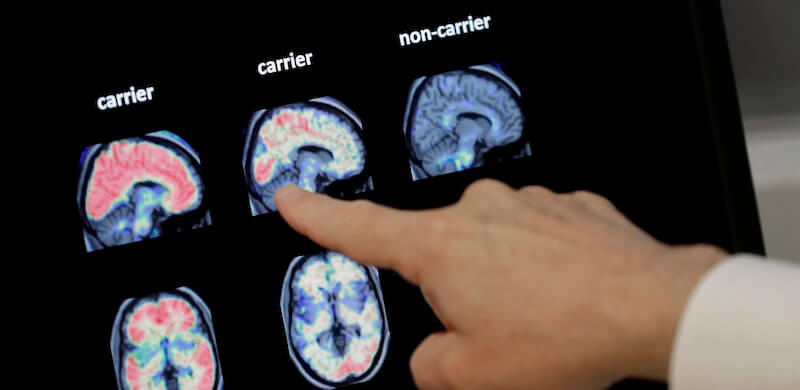
L’approvazione negli Stati Uniti dell’Aduhelm (aducanumab), un farmaco che dovrebbe rallentare gli effetti del morbo di Alzheimer, sta facendo discutere medici e ricercatori non solo per i dubbi sulla sua efficacia, ma anche per il modo in cui è stato approvato. Secondo Biogen, l’azienda farmaceutica che lo produce, potrà migliorare la vita a milioni di persone che hanno ricevuto una diagnosi precoce di Alzheimer, e che sono quindi a rischio di perdere progressivamente la memoria, la capacità di riconoscere i propri cari e di capire dove si trovano. Secondo i più critici difficilmente migliorerà le cose e offrirà evidenti benefici.
I farmaci attualmente disponibili cercano di trattare i sintomi dell’Alzheimer, ma non riescono a fare molto contro la malattia, soprattutto nelle sue forme più avanzate. L’Aduhelm è stato sviluppato seguendo un approccio diverso: agire contro la causa della malattia in modo che questa progredisca più lentamente. Per farlo, il principio attivo interviene sulla betamiloide, una proteina che causa un accumulo di placche nei neuroni rendendoli via via meno reattivi e funzionali. Da tempo i ricercatori ritengono che questa proteina sia una, se non la principale, causa dell’Alzheimer, anche se tenerla sotto controllo è difficile e ci sono dubbi sul suo ruolo nella malattia.
L’Aduhelm non cura quindi l’Alzheimer e non ha nemmeno la capacità di ridurre gli effetti che si sono ormai manifestati, per esempio una perdita considerevole delle capacità cognitive di un malato.
Difficoltà e test
Biogen non è l’unica azienda ad avere seguito la strada della betamiloide per provare a trattare l’Alzheimer. Negli anni ci hanno provato diverse altre aziende farmaceutiche comprese alcune delle più grandi al mondo come Pfizer, Roche, Merck ed Eli Lilly (di quest’ultima si era parlato molto lo scorso anno per i suoi anticorpi monoclonali contro la COVID-19). Avevano tutte fallito nello sviluppare una soluzione in grado di eliminare gli accumuli di betamiloide.
Nonostante l’alto tasso di fallimento, i ricercatori di Biogen proseguirono le ricerche sviluppando un farmaco più potente rispetto alle versioni della concorrenza, e almeno in linea teorica in grado di eliminare con maggiore efficacia le placche causate dalla proteina. L’azienda orientò inoltre l’impiego del farmaco nei pazienti con sintomi ancora lievi e segno di un Alzheimer incipiente.
Le due prime fasi (su tre) dei test clinici per valutare la sicurezza del farmaco diedero esiti incoraggianti e Biogen circa cinque anni fa avviò la terza fase, con un numero più ampio di volontari.
Furono organizzati due test clinici identici, ciascuno dei quali con i volontari divisi in due gruppi: uno avrebbe ricevuto il farmaco vero e proprio, mentre l’altro una sostanza che non fa nulla (placebo). Dopo i primi test, la sperimentazione sui pazienti fu interrotta nella primavera del 2019, quando un gruppo di valutazione indipendente concluse che l’Aduhelm non stesse portando benefici ai pazienti. Il farmaco sembrava essere inutile e destinato a finire insieme ai numerosi altri fallimenti degli ultimi 20 anni nella ricerca di nuove terapie contro l’Alzheimer.
Analisi ed efficacia
Per Biogen il rischio di avere speso inutilmente svariati milioni di dollari si stava facendo sempre più concreto. Le cose cambiarono nell’autunno del 2019, quando l’azienda farmaceutica presentò una nuova analisi basata su nuovi dati che non erano stati ancora presi in considerazione. Evidenziava un rallentamento nell’avanzare dei problemi cognitivi in alcuni individui sottoposti alla terapia. La differenza tra l’impiego del farmaco e del placebo era però estremamente bassa: meno di un punto su 18.
Mentre i risultati sul rallentamento della malattia erano deludenti, le ricerche sui due test clinici avevano indicato la capacità dell’Aduhelm di ridurre gli accumuli di betamiloide da alcune aree del cervello. La riduzione era stata di quasi un terzo rispetto ai volontari trattati con un placebo. Era stato però riscontrato un anomalo accumulo di fluidi (edema) a livello cerebrale nel 40 per cento circa dei partecipanti, una condizione rischiosa e piuttosto dolorosa.
Nell’estate del 2020, Biogen presentò alla FDA gli esiti dei test clinici, nonostante questi fossero stati sospesi temporaneamente e avessero comunque portato a conclusioni difficili da interpretare. La scelta fu accolta con non poche perplessità da parte di altri ricercatori ed esperti. Nell’autunno dello stesso anno una commissione nominata dalla FDA concluse che i dati forniti non fossero sufficienti per dimostrare la capacità dell’Aduhelm di rallentare la degenerazione cognitiva nei malati di Alzheimer. Un’altra commissione di esperti arrivò a conclusioni meno nette, ma nel frattempo emersero alcuni conflitti di interessi tra il principale responsabile della revisione per l’FDA e Biogen.
Approvazione condizionale
Nonostante i pareri negativi di una delle commissioni, l’FDA ha concluso che fosse comunque opportuna l’approvazione dell’Aduhelm, anche alla luce della mancanza di nuovi farmaci contro l’Alzheimer negli ultimi decenni. L’approvazione è però sotto condizione, una scelta insolita per l’FDA e che ha fatto ulteriormente discutere.
Il farmaco è stato approvato sulla base della sua capacità di eliminare la betamiloide, come emerso in entrambi gli studi, ma per poter continuare a venderlo Biogen dovrà terminare uno studio clinico che confermi i benefici per le capacità cognitive derivanti dalla rimozione della proteina. Nel caso in cui lo studio portasse a conclusioni diverse, l’FDA potrebbe annullare l’approvazione da poco concessa.
La scelta dell’autorità di controllo statunitense ha sorpreso molti osservatori e potrebbe avere implicazioni in futuro nel processo di approvazione di altri farmaci. L’FDA ha di fatto sancito che in alcune circostanze si possa approvare un nuovo medicinale sulla base delle sue potenzialità, anche se non ha ancora mostrato di avere la capacità di produrre benefici. Lo stesso criterio potrebbe essere applicato per farmaci di nuova generazione orientati a curare o trattare malattie gravi, per le quali a oggi non esistono rimedi efficaci. Per Biogen, intanto, potrebbe essere un grande affare.
Prezzo
Negli Stati Uniti si stima che l’Alzheimer interessi circa 6 milioni di persone (su una popolazione di 330 milioni), nella maggior parte dei casi anziani, che non sempre possono accedere alle terapie più avanzate. Oltre ai problemi economici e di copertura delle assicurazioni sanitarie, alcuni farmaci non possono essere impiegati su tutti i pazienti a causa dei loro effetti collaterali. La risposta alle terapie varia inoltre sensibilmente, con qualche effetto positivo nel breve periodo su alcuni sintomi.
L’Aduhelm richiede una somministrazione al mese, che deve essere effettuata tramite flebo in un ambulatorio o in ospedale, sotto la supervisione del personale sanitario. Biogen stima che un trattamento per un anno abbia un prezzo di listino di 56mila dollari. La cifra si riduce sensibilmente a seconda della propria copertura assicurativa, e si stima che il costo per i pazienti potrebbe aggirarsi intorno ai 10-25mila dollari all’anno. A questi prezzi, l’Aduhelm rientra tra i farmaci ad accesso tramite medici di medicina generale più costosi mai messi in commercio negli Stati Uniti.
In linea di massima tutti i pazienti con diagnosi di Alzheimer potranno accedere al nuovo trattamento, salvo avere le disponibilità economiche per farlo e le adeguate coperture assicurative. Prima di avviare il trattamento, ogni paziente dovrà comunque essere sottoposto a un esame di diagnostica per immagini per la valutazione delle sue condizioni cerebrali.
Secondo gli analisti, Biogen potrebbe ricavare tra i 5 e i 6 miliardi di dollari l’anno dall’Aduhelm, ipotizzando che il prezzo del farmaco si stabilizzi intorno ai 10mila dollari una volta che il sistema di produzione e distribuzione sarà a pieno regime. La stima è basata su uno scenario in cui un quinto circa dei malati di Alzheimer negli Stati Uniti utilizzi regolarmente il nuovo farmaco.
Le cose per Biogen potrebbero invece complicarsi se i nuovi dati richiesti dalla FDA mostrassero un’efficacia ridotta o assente nel rallentare la progressione dell’Alzheimer. Oltre a perdere l’approvazione dell’autorità di controllo, l’azienda farmaceutica si troverebbe a dover risolvere contenziosi con pazienti e società di assicurazioni.
Una malattia, pochi progressi
Ogni anno le principali aziende farmaceutiche investono l’equivalente di centinaia di milioni di euro per sviluppare e testare nuove molecole, alla ricerca dei candidati più promettenti per ottenere farmaci di nuova generazione davvero efficaci contro il morbo di Alzheimer. Nonostante gli sforzi e le grandi risorse investite, negli ultimi 20 anni non sono emersi farmaci tali da costituire un punto di svolta per tenere sotto controllo la malattia, nonostante questa interessi milioni di persone e abbia un lungo decorso.
La malattia si manifesta solitamente dopo i 65 anni con sintomi precoci come l’incapacità di ricordare eventi recenti. Con l’avanzare della malattia, e dell’età, i sintomi peggiorano e si hanno spesso disorientamento, repentini cambi di umore, depressione e una crescente difficoltà nel ricordare. Secondo l’Organizzazione Mondiale della Sanità (OMS), in tutto il mondo ci sono 50 milioni di persone che soffrono di demenza, con l’Alzheimer come principale causa nel 60-70 per cento dei casi.



