C’è un primo intoppo per il remdesivir contro il coronavirus
Una ricerca preliminare pubblicata per errore dall'OMS indica scarsi benefici del farmaco su cui ci sono grandi aspettative, ma lo studio ha diversi difetti
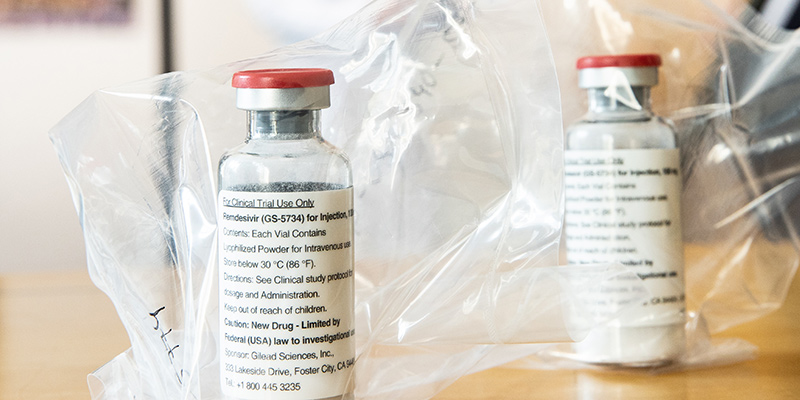
Nelle ultime ore diversi giornali hanno pubblicato articoli sul farmaco antivirale remdesivir, citando uno studio preliminare pubblicato in Cina secondo il quale il farmaco avrebbe deluso le aspettative nel trattamento di alcuni pazienti con la COVID-19. La ricerca contiene in effetti alcuni elementi che mettono in dubbio l’utilità del trattamento contro il coronavirus, ma deve essere ancora sottoposta a revisione e non offre comunque un quadro completo: era stata interrotta prematuramente dai ricercatori, prima che fosse condotta su un numero significativo di pazienti.
A questo stadio, ricerche del genere passano di solito inosservate, proprio perché non forniscono ancora tutti i dati necessari per essere ritenute affidabili. Lo studio è invece finito su molti giornali e siti a causa di un errore da parte dell’Organizzazione Mondiale della Sanità (OMS), che ne ha pubblicato il riassunto introduttivo sul proprio sito, procedendo poi dopo qualche ora alla sua rimozione. La ricerca è stata notata da esperti e giornalisti e in poco tempo ha ricevuto grandi attenzioni, anche se si tratta di un documento preliminare e in attesa di essere rivisto da altri esperti.
Una portavoce dell’OMS ha spiegato: “Gli autori hanno fornito una bozza all’Organizzazione che l’ha pubblicata per errore sul proprio sito, ritirandola una volta scoperto l’errore. La bozza è ora sotto revisione alla pari e siamo in attesa della sua versione finale, sulla quale l’OMS farà le proprie valutazioni”.
Il remdesivir è un farmaco antivirale di recente introduzione, sviluppato dall’azienda farmaceutica Gilead negli anni delle epidemie causate dall’Ebola in Africa occidentale tra il 2013 e il 2016. La sua sperimentazione aveva portato a risultati che sembravano incoraggianti, ma un suo impiego su più grande scala contro l’Ebola rivelò una scarsa efficacia rispetto ad altre soluzioni. Il farmaco era stato anche sperimentato per trattare alcuni casi di SARS e MERS, sindromi respiratorie causate da altri coronavirus, con risultati che erano stati definiti incoraggianti.
Come suggerisce la parola, un antivirale serve per rallentare la velocità con la quale i virus si replicano all’interno di un organismo, dando qualche possibilità in più al sistema immunitario di contrastare l’infezione. Farmaci di questo tipo sono piuttosto potenti e possono avere numerosi effetti collaterali, per questo devono essere somministrati sotto attenta sorveglianza da parte dei medici.
Considerate le precedenti esperienze con SARS e MERS, negli ultimi mesi il remdesivir è stato oggetto di numerose ricerche per valutarne l’efficacia nei trattamenti contro la COVID-19. Sono attualmente in corso numerosi studi e la ricerca cinese non fornisce quindi una risposta definitiva circa la sua utilità.
Stando al riassunto erroneamente pubblicato dall’OMS, lo studio condotto in Cina non ha rilevato particolari differenze tra un gruppo di pazienti trattati con il remdesivir e uno di controllo sottoposto alle terapie più comuni impiegate contro la COVID-19. Dopo un mese di trattamento, il 13,9 per cento dei pazienti nel gruppo sotto remdesivir è morto, contro il 12,8 per cento dei pazienti nel gruppo di controllo. La differenza è stata definitiva “statisticamente non rilevante” dai ricercatori. Ma lo studio presenta alcuni altri problemi.
Inizialmente, i ricercatori avevano previsto di condurre la loro ricerca clinica su circa 450 pazienti. Il prerequisito per ogni nuovo partecipante era di avere sviluppato i sintomi della COVID-19 entro i 12 giorni precedenti. Man mano che diventavano disponibili, i nuovi partecipanti venivano suddivisi casualmente nel gruppo che avrebbe ricevuto il remdesivir e in quello di controllo con le normali terapie e la somministrazione di un placebo (un finto farmaco): come avviene spesso con questo tipo di studi, ai pazienti non veniva comunicato in quale gruppo si trovassero.
Lo studio aveva come obiettivo principale la valutazione dell’efficacia del remdesivir rispetto a un placebo nel migliorare i sintomi dopo 28 giorni di trattamento. Per la valutazione era previsto un sistema a punti: da 1 per la dimissione dei pazienti a 6 nel caso della loro morte. I ricercatori avevano fissato a 2 il punteggio minimo per attribuire un qualche effetto positivo del remdesivir.
Nella pratica le cose sono andate diversamente da come avevano sperato i ricercatori, soprattutto a causa della difficoltà di trovare un numero sufficiente di pazienti con le giuste caratteristiche in Cina. La ricerca ha coinvolto nel complesso 237 persone, circa la metà di quanto previsto ed è stata poi interrotta prematuramente, proprio a causa delle difficoltà nel trovare nuovi volontari. Sulla base dei dati disponibili, i ricercatori hanno comunque segnalato di non avere rilevato differenze significative tra i due gruppi, notando una maggiore lentezza nel miglioramento dei sintomi per i pazienti sotto remdesivir.
L’azienda farmaceutica Gilead ha risposto all’errore dell’OMS dicendo che il riassunto conteneva comunque alcune “caratterizzazioni inappropriate” dello studio cinese, non rendendo chiaro a sufficienza che fosse stato interrotto prematuramente e che non avesse portato a conclusioni statisticamente significative. La società ha poi rilevato come alcuni dati nello studio indichino comunque possibili benefici da parte del remdesivir, nel caso di una somministrazione del farmaco nei primi stadi della malattia.
Gilead nelle ultime settimane ha avviato diverse collaborazioni con università, cliniche ed enti di ricerca per valutare gli effetti del suo farmaco sui malati di COVID-19. Un primo studio condotto presso l’Università di Chicago ha dato risultati preliminari definiti incoraggianti, anche se è stato svolto con metodologie diverse e senza prevedere un confronto tra pazienti sotto remdesivir e trattati con normali terapie.



